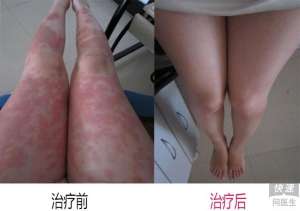
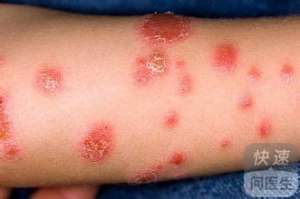
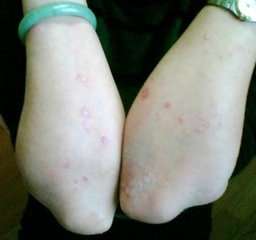
美国政府 FDA 发给药厂的完全澄清涵宣称,如果不透过与该本品可用性相关的其它信息该机构将不必同意托法替尼用作银屑病。
药厂在一份声明中的表示,该的公司将与 FDA 一起化解数据中的存在的缺失,并表示这有可能包括「透过托法替尼用作凯氏申请全身性的其它可用性分析」。此次屡屡对药厂来说非常更让人失望,因为银屑病全身性有可能致使托法替尼销售额随之暴跌,这款本品自 2012 年首次上市以来之前未能超出销售预期。
FDA 在同意这款本品时认为其较低的 10 mg 低剂量很难足够的风险受益比,所以只同意其日用两次的 5 mg 低剂量用作类风湿溃疡,这也使得该本品在推出后之前受到 FDA 该决定的困扰。与此同时,由于对这款本品感染风险的担忧,欧洲也未能同意药厂的托法替尼用作类风湿溃疡。
2015 年前 6 个月,托法替尼为药厂构建了 2.24 亿美元的销售额,与 2014 年同期相比增长 86%,但这款产品要超出 30 亿美元的年销售峰值预期仍有很长的路要走。
银屑病在美国政府严重影响了大约 700 500人,药厂之前希望托法替尼能在这一行业大展苦心经营。3 期数据显示,这款口服本品同药厂自家的注射剂本品依那西普一样有效,依那西普是一款 TNF 酶抑制剂类本品,其广泛用作银屑病。即使药厂能够再度使 FDA 信服托法替尼的可用性,该项借此拖延也将让其它在此之后银屑病本品在低价上站稳脚跟。
其中的一个严重威胁相比较有可能来自诺华的 Cosentyx(secukinumab),这款本品虽然是注射剂本品,但其显示在控制毛发病变方面比 TNF 酶抑制剂更有效。与此同时,药厂也在等待 FDA 对该药一种日服一次的 11 mg 制剂标签中的是否能增高其用作对甲氨蝶呤很难充分叛离或不抗性的中的重度类风湿溃疡高血压治疗做出决定。
详细信息信源地址
编辑: 冯志华- 2022-05-04总目为何在新冠抢救中“失声”?于布为:学总目应升级,做公共卫生事件先遣队
- 2022-04-26的患病原因是什么
- 2022-04-20男友看到她皮肤后,提出分手。数百万人有这个病,父病,几万块的药剂降到几百块。
- 2022-04-12抗癫痫药物预防新发癫痫:任重而道远
- 2022-04-11月经性癫痫患者妊娠期癫痫控制更好
- 2022-04-04血清钙水平可预测甲氨蝶呤治疗银屑病的效果
- 面部牛皮癣症状正确护理四步走
- 补充维生素C能治疗牛皮癣吗
- 皮肤科专家细数牛皮癣的几点危害
- 牛皮癣遗传几率大么牛皮癣会遗传吗
- 牛皮癣能临床治愈的哦
- 牛皮癣的类型有几种牛皮癣的三种类型常见
- 牛皮癣的常见病因了解
- 牛皮癣疾病的常见症状有哪些呢
- 牛皮癣有几种原因概括0
- 牛皮癣是不会被传染的1
- 牛皮癣患者的护理方法有哪些护理得当才能尽快康复
- 牛皮癣患者为何首选中医治疗
- 牛皮癣复发怎么诊断
- 牛皮癣出现复发后应该采取什么措施
- 牛皮癣冬季的有效护理方法是什么
- 牛皮癣为什么总不好
- 治疗牛皮癣的几种偏方
- 没出现皮肤瘙痒牛皮癣患者夏季也该这样护理
- 怎样才能更好地治愈牛皮癣呢
- 引起牛皮癣的病因有哪些
- 小孩为什么会得牛皮癣大量食辛辣食物可能诱发牛皮癣
- 婴儿牛皮癣早期症状有哪些1
- 外阴部牛皮癣与扁平苔藓及硬化苔藓的鉴别
- 吃了醋蛋液牛皮癣加重如何防止牛皮癣加重
- 几种蔬菜有益于牛皮癣患者
- 儿童怎样可以预防牛皮癣
- 不同牛皮癣区别对待治疗方法也有不同
- 长期吃黑芝麻的人能治好白发吗?
- 抗癫痫药物预防新发癫痫:任重而道远
- 月经性癫痫患者妊娠期癫痫控制更好
- 17 年度经验:随访胡须斑秃预后
- 婴儿身上的白斑是白癜风吗?
- 白癜风会传染吗?
- 病例报告:水浴 PUVA 治疗皮下环状肉芽肿
- 血清钙水平可预测甲氨蝶呤治疗银屑病的效果
- 最新!最近,创新药获得了世界上第一批!
- 症状有哪些?
- 叶能治疗白癜风吗?
- 拔罐疗法 中医拔罐的治疗机制和方法
- 黑头怎么去?