新泽西州 FDA 的一个顾问委员则会月末说明,只要减轻行凶危险性的相关措施即便如此,瓦兰特国际上化工公司的面部银屑病实验抗生素 Brodalumab 不宜获得审批。FDA 虽然没有义务遵循其顾问委员则会的建议,但他们通常则会这样做。
在这款抗生素的临床试验之前,有 6 名病患在整个的项目之前行凶,4 名病患在银屑病研究之前,1 名病患在类风湿病征研究之前,外 1 名病患是在银屑病官能病征研究之前。即使这样,顾问委员则会仍以 18 比 0 的投票结果赞成这款抗生素获得审批,称该抗生素的获益超过了潜在的危险性。
18 名顾问领导者之前,14 名领导者赞成这款抗生素只能值得注意稳固的危险性管理项目使用,这些危险性管理项目胜过了标签之前包含的反馈。它们也许还包括抗生素范本及为保健供不宜商获取交流计划。
顾问一个小组领导者说明,银屑病对新药有生产力,他们想让 Brodalumab 作为一种选择供病人使用。对于如何减轻行凶危险性,他们获取了各种建议,还包括黑框无视及收集病人图表的病人申请及更明确地评论者行凶危险性。
一些一个小组领导者认为病人申请不宜予以强制,其他一个小组领导者认为病人申请不宜自愿。一些一个小组领导者认为任何病人申请将对评论者这款抗生素造成避免的障碍,也不也许看出行凶危险性的正确地估计。Valeant 自己有一个危险性管理提议,还包括直接参与病人申请,另外要强化交流,但不填充黑框无视。
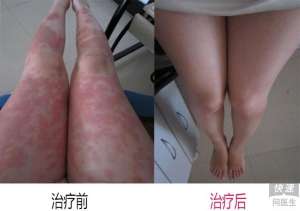
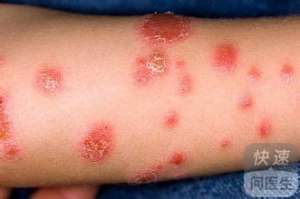
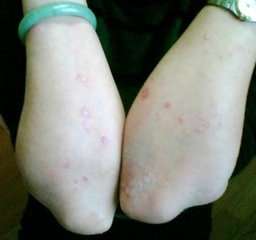
Brodalumab 通过阻绝一种叫白介素-17 的蛋白受体来缓解炎症。几个其它的白介素-17 抑制现在纳斯达克,还包括诺华的 Cosentyx 与礼来的 Taltz。这款抗生素也将永定后下的依那西普、Harvey的英利昔单抗及艾伯维的修卡夫后下行公平竞争。据新泽西州面部病学则会获取的反馈,新泽西州大约有 750 万人致使银屑病的拖累。这种疾病的特性是外侧、鳞状面部白斑,它也许与其它疾病相关,还包括糖尿病与心脏疾病。
Brodalumab 最初由阿斯利康与安后下开发设计。2015 年 5 月,安后下由于行凶危险性从这一抗生素的协力之前退出。阿斯利康后来把这款抗生素的在世界上权利许可给 Valeant,即使如此一年,这款抗生素的最小值大跌,其高抗生素价格及与专项药店紧张的关系广受指责。
察看信源IP
主笔: 冯志华上一页:脓胞型银屑病诊断和化疗
下一页:患者的饮食医疗
- 2022-05-04总目为何在新冠抢救中“失声”?于布为:学总目应升级,做公共卫生事件先遣队
- 2022-04-26的患病原因是什么
- 2022-04-20男友看到她皮肤后,提出分手。数百万人有这个病,父病,几万块的药剂降到几百块。
- 2022-04-12抗癫痫药物预防新发癫痫:任重而道远
- 2022-04-11月经性癫痫患者妊娠期癫痫控制更好
- 2022-04-04血清钙水平可预测甲氨蝶呤治疗银屑病的效果
- 面部牛皮癣症状正确护理四步走
- 补充维生素C能治疗牛皮癣吗
- 皮肤科专家细数牛皮癣的几点危害
- 牛皮癣遗传几率大么牛皮癣会遗传吗
- 牛皮癣能临床治愈的哦
- 牛皮癣的类型有几种牛皮癣的三种类型常见
- 牛皮癣的常见病因了解
- 牛皮癣疾病的常见症状有哪些呢
- 牛皮癣有几种原因概括0
- 牛皮癣是不会被传染的1
- 牛皮癣患者的护理方法有哪些护理得当才能尽快康复
- 牛皮癣患者为何首选中医治疗
- 牛皮癣复发怎么诊断
- 牛皮癣出现复发后应该采取什么措施
- 牛皮癣冬季的有效护理方法是什么
- 牛皮癣为什么总不好
- 治疗牛皮癣的几种偏方
- 没出现皮肤瘙痒牛皮癣患者夏季也该这样护理
- 怎样才能更好地治愈牛皮癣呢
- 引起牛皮癣的病因有哪些
- 小孩为什么会得牛皮癣大量食辛辣食物可能诱发牛皮癣
- 婴儿牛皮癣早期症状有哪些1
- 外阴部牛皮癣与扁平苔藓及硬化苔藓的鉴别
- 吃了醋蛋液牛皮癣加重如何防止牛皮癣加重
- 几种蔬菜有益于牛皮癣患者
- 儿童怎样可以预防牛皮癣
- 不同牛皮癣区别对待治疗方法也有不同
- 长期吃黑芝麻的人能治好白发吗?
- 抗癫痫药物预防新发癫痫:任重而道远
- 月经性癫痫患者妊娠期癫痫控制更好
- 17 年度经验:随访胡须斑秃预后
- 婴儿身上的白斑是白癜风吗?
- 白癜风会传染吗?
- 病例报告:水浴 PUVA 治疗皮下环状肉芽肿
- 血清钙水平可预测甲氨蝶呤治疗银屑病的效果
- 最新!最近,创新药获得了世界上第一批!
- 症状有哪些?
- 叶能治疗白癜风吗?
- 拔罐疗法 中医拔罐的治疗机制和方法
- 黑头怎么去?